复星医药自研1类肺癌创新药复瑞替尼上市申请获受理
2025年3月6日,复星医药宣布,自主研发的1类新药丁二酸复瑞替尼胶囊(项目代号:SAF-189,Foritinib,以下简称“该新药”)的上市申请于近日获国家药品监督管理局受理。该新药主要用于治疗ALK阳性非小细胞肺癌、ROS1阳性非小细胞肺癌等,本次申报适应症为用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者的治疗。
复瑞替尼(Foritinib)是一种在研的高效、具有CNS高渗透性的ALK/ROS1抑制剂,截至目前的临床研究显示,该新药在ALK阳性的非小细胞肺癌晚期患者中,展现出良好的临床疗效,对中枢神经系统转移灶疗效显著,且安全性良好。截至目前,该新药的另一适应症用于治疗非小细胞肺癌(ROS1+)于中国境内已完成II期临床研究。
在2024年世界肺癌大会(WCLC)期间,复瑞替尼治疗ALK阳性非小细胞肺癌的III期REMARK研究的期中分析结果以最新突破性摘要(LBA)形式公布。在该研究中,复瑞替尼治疗组的PFS相较于克唑替尼减少了77%疾病进展或死亡的风险(PFS NR vs 13.93m,HR 0.23, 95% CI 0.14-0.38),表明复瑞替尼是极具前景的用于治疗ALK阳性非小细胞肺癌的创新药物。
研究方法
REMARK研究是一项开放标签、随机、III期临床研究,纳入了既往未经治疗的ALK阳性晚期NSCLC患者。患者根据基线ECOG评分(0/1 vs 2)和是否发生CNS转移进行分层分析,并按1:1比例随机分为接受复瑞替尼治疗(160 mg,每日一次)或克唑替尼治疗(250 mg,每日两次)。研究主要终点为由独立评审委员会(IRC)评估的无进展生存期(PFS),次要终点包括由研究者(INV)评估的PFS和客观应答率(ORR);由IRC和INV评估的应答时间(TTR)和应答持续时间(DOR);由IRC评估的颅内 ORR(C-ORR)、颅内TTR(C-TTR)、颅内DOR(C-DOR)和所有受试者至CNS进展时间(CNS-TTP);以及总生存期(OS)和安全性。
研究结果
从2020年12月至2022年3月,该研究共招募275例患者,其中139例接受复瑞替尼治疗,136接受克唑替尼治疗。截至2024年3月,中位随访时间为16.7个月。研究发现,复瑞替尼治疗组的PFS相较于克唑替尼治疗组具有显著改善,克唑替尼治疗组的中位PFS为13.93个月,而复瑞替尼治疗组尚未达到(HR 0.23, 95% CI 0.14-0.38, 图1)。
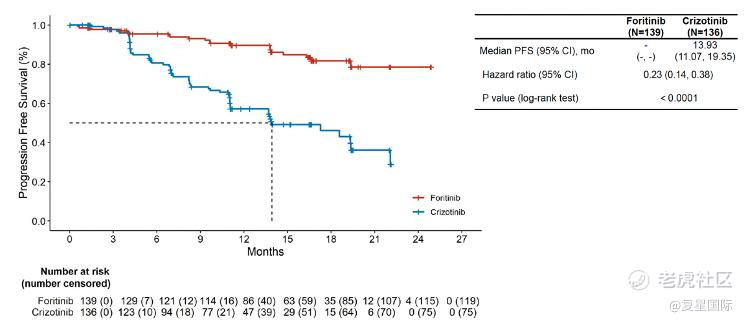
此外,相比于克唑替尼,复瑞替尼显著降低CNS进展风险。克唑替尼治疗组中位CNS-TTP为19.32个月,而复瑞替尼组尚未达到(HR 0.04, 95% CI 0.01-0.14)。另外,复瑞替尼有改善OS的趋势(HR 0.60, 95% CI 0.30-1.20)。
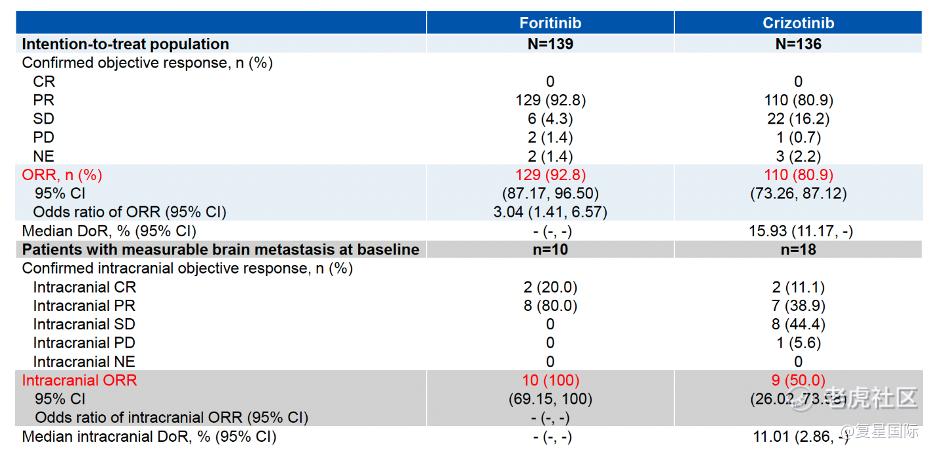
同时,研究结果显示复瑞替尼治疗组的ORR达到92.8%,相较于克唑替尼治疗组提高12%(P=0.0035);且对于基线脑转移的患者,复瑞替尼治疗组的颅内ORR可达到100%,而克唑替尼治疗组为50%(表1)。
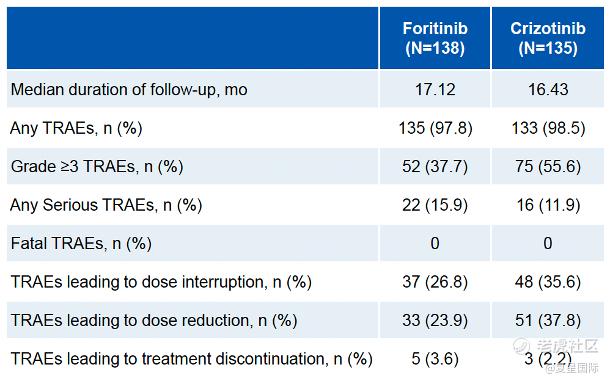
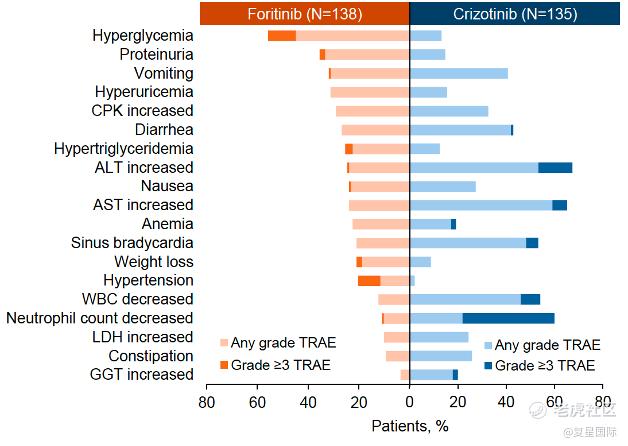
安全性方面,复瑞替尼治疗组患者3/4级治疗相关不良事件(TRAEs)的发生率为37.7%,克唑替尼治疗组为55.6%。复瑞替尼治疗后最常见的3/4级TRAEs为高血糖、高血压和QT间期延长。复瑞替尼治疗组未观察到间质性肺病或视力下降。两组患者治疗后均未报告致死性TRAE(表2&图2)。
综上,该研究结果表明复瑞替尼疗效良好,相比于克唑替尼治疗可使PFS显著改善,使CNS进展风险降低,且其安全性可控,治疗后未出现新的安全性信号。复瑞替尼的出现有望突破目前ALK阳性NSCLC治疗所面临的临床困难,为NSCLC患者带来新的治疗选择。
参考文献:
1. Xiong A. Randomized, Open-label, Phase III Study of SAF-189s Versus Crizotinib in First-Line ALK-Positive Advanced Non-Small Cell Lung Cancer (NSCLC). WCLC 2024.
2. Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024;74(3):229-263. doi:10.3322/caac.21834
3. Han B, Zheng R, Zeng H, et al. Cancer incidence and mortality in China, 2022. J Natl Cancer Cent. 2024;4(1):47-53. Published 2024 Feb 2. doi:10.1016/j.jncc.2024.01.006.
4. Bareschino MA, Schettino C, Rossi A, et al. Treatment of advanced non small cell lung cancer. J Thorac Dis. 2011;3(2):122-133. doi:10.3978/j.issn.2072-1439.2010.12.08.
5. Gou LY, Wu YL. Prevalence of driver mutations in non-small-cell lung cancers in the People's Republic of China. Lung Cancer (Auckl). 2014;5:1-9. Published 2014 Feb 12. doi:10.2147/LCTT.S40817.
6. Yang JJ, Zhou J, Liu SM, et al. Foritinib in advanced ROS1-rearranged non-small-cell lung cancer in China: a multicentre, open-label, single-arm, phase 2 study. Lancet Respir Med. 2024;12(9):671-680. doi:10.1016/S2213-2600(24)00171-1.
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。



